第六十二章
机制推演: 病毒不仅修改了染色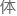 数量,还对胚胎发育程序进行了“后门植入”。
数量,还对胚胎发育程序进行了“后门植入”。
原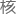 形成: 随后迅速出现雌雄原
形成: 随后迅速出现雌雄原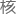 (Pronucleus)
(Pronucleus) 合迹象。
合迹象。
2. 机制提示(Mechanism Hypothesis):
染色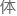 兼容
兼容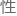 : 因感染动物的单倍
: 因感染动物的单倍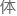 数已被修饰为 n = 23(与人类完全一致),且关键染色
数已被修饰为 n = 23(与人类完全一致),且关键染色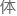 区段存在高度同源或插入
区段存在高度同源或插入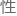 “
“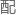 对元件”(Pairing Elements)。这使得减数分裂后的异源
对元件”(Pairing Elements)。这使得减数分裂后的异源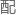 子之间,能实现
子之间,能实现 确的染色
确的染色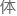
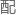 对与初期合子的基因组稳定。
对与初期合子的基因组稳定。
三、 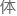 内授
内授 与自我实验(In Vivo / Self-Experimentation)
与自我实验(In Vivo / Self-Experimentation)
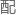 子来源: 人类卵母细胞(冷冻复苏/新鲜采集) 筛选后的感染山羊
子来源: 人类卵母细胞(冷冻复苏/新鲜采集) 筛选后的感染山羊 子。
子。
1. 观测结果(Observations):
表达增强元件”的富集。
甲基化重编程: 在与生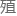 发育相关的调控区,观察到显著的去甲基化迹象。
发育相关的调控区,观察到显著的去甲基化迹象。
病毒辅助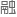 合: 病毒重组元件在
合: 病毒重组元件在 子
子 表面高表达类合胞
表面高表达类合胞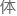
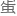 白(Syncytin-like proteins)。这种“分子胶水”极大降低了
白(Syncytin-like proteins)。这种“分子胶水”极大降低了 卵结合的能垒,从而实现了强制
卵结合的能垒,从而实现了强制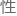 、高效率的跨物种受
、高效率的跨物种受 。
。
超速受 : 混合后 30 分钟内,显微镜下即观察到数例
: 混合后 30 分钟内,显微镜下即观察到数例 子成功诱发
子成功诱发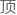
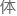 反应,穿透透明带并与卵
反应,穿透透明带并与卵 发生
发生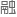 合。
合。
统计数据: 本组受 效能估算约为人类同源对照组的 2.7 倍。
效能估算约为人类同源对照组的 2.7 倍。
过程数据: 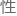 交后立即采集
交后立即采集 颈黏
颈黏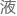 与血清样本。镜检显示,
与血清样本。镜检显示, 子在
子在 颈黏
颈黏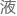 中的活力指数与
中的活力指数与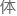 外优化环境结果高度一致,未受到免疫系统攻击。
外优化环境结果高度一致,未受到免疫系统攻击。
受试者: 林岚(Lin Lan, Investigator)
妊娠确认:
指标: 血清学 β-hCG 飙升;经阴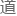 超声
超声
效率评估: 总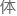 受
受 率与早期胚胎发育率,显著高于常规人类 IVF 对照组。
率与早期胚胎发育率,显著高于常规人类 IVF 对照组。
二、 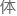 外受
外受 模拟验证(IVF Simulation & Viability)
模拟验证(IVF Simulation & Viability)
实验环境: P3 级生物安全柜(Class III BSC),模拟输卵 微环境。
微环境。
最终目的: 确保杂交后代虽然在母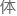 内孕育,但其表型(外貌、力量、本能)将完全偏向兽类,而非人类。人类女
内孕育,但其表型(外貌、力量、本能)将完全偏向兽类,而非人类。人类女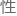 的子
的子 ,仅仅被降格为一个提供营养的高级孵化箱。
,仅仅被降格为一个提供营养的高级孵化箱。
方法: 为验证真实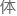 内的着床环境,本人自愿进行受试
内的着床环境,本人自愿进行受试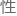 交
交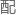 (Unprotected Coitus)以获取一手临床数据。
(Unprotected Coitus)以获取一手临床数据。
卵裂启动: 培养 12 小时后,若干胚胎成功分裂至 二细胞期(2-cell stage),形态饱满,无碎片化现象。
【附件:扫描文档 LX-05(第 3 页 ・ 临床结论)】
时间: 交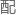 后 14 天(Post-Coital Day 14)。
后 14 天(Post-Coital Day 14)。
显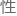 压制: 这种修饰旨在破坏人类卵母细胞的母系印记,极大提高父系(山羊)基因在胚胎发育中的主导
压制: 这种修饰旨在破坏人类卵母细胞的母系印记,极大提高父系(山羊)基因在胚胎发育中的主导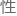 。
。
【附件:扫描文档 LX-05(第 2 页 ・ 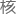 心验证)】
心验证)】